研究をラボから臨床へと前進させるために
研究を臨床への進展に近づけるために必要なデータを提供するよう専門性を持つ科学者によって設計された免疫細胞スクリーニングサービス
信頼性の高いin vitro免疫細胞モデルデータにより、新しい創薬標的を明らかにし、より迅速な開発する治療方針の決定が可能になります。Revvityでは、初代免疫細胞における生理学的に関連性の高いゲノム編集の評価を可能にする機能的データを揃えた先進的なCRISPRを用いたアプローチを提供しています。当社のImmuSignature™アッセイは、複数のドナーサンプルを用いることでドナー間のばらつきに対処し、リード治療薬の最適化を迅速かつ有意義に進めることができます。
ImmuSignatureスクリーニングによる化合物の免疫原性の評価
リード治療薬の最適化は、医薬品開発における重要なステップであり、困難を伴うものです。初代免疫細胞を評価する際には、複雑で時間のかかる手順となることがよくあります。当社の初代免疫細胞スクリーニング ImmuSignature アッセイは、in vitroで免疫微小環境をシミュレートした環境で化合物をスクリーニングすることができ、約3週間でヒットの高品質のリードへの移行をサポートします。
プロジェクトのあらゆる段階で、当社のPreclinicalサービスチームと連携を
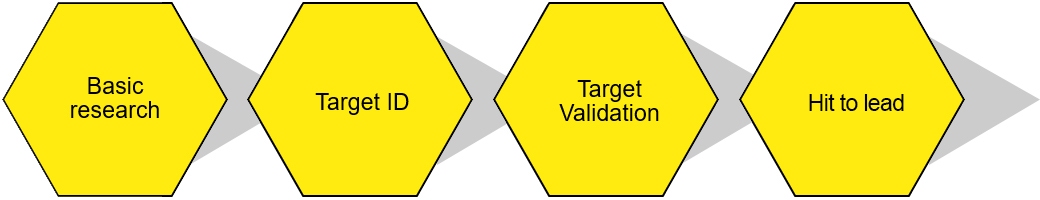
免疫細胞スクリーニングプロジェクト
ヒトの初代リンパ系および骨髄系細胞におけるゲノムCRISPRノックアウトスクリーニングにより、機能的データで関連遺伝子を同定
- ガイドRNAを作成し、ご研究の疾患モデルに関連する遺伝子を同定
- 細胞表面マーカーとタンパク質放出に関する情報を取得
- ハイスループットでイメージングおよび機能的データを探索
- T細胞、B細胞、マクロファージ、または単球におけるアレイ化およびプール化スクリーニング
ImmuSignatureアッセイによる化合物スクリーニング
標準化された化合物スクリーニングアッセイを使用して、免疫細胞ベースの環境におけるリード治療薬の有効性を迅速に評価
- 薬剤候補の免疫学的影響を解析
- 免疫毒性解析を通じて安全性を評価
- T細胞の増殖や制御性T細胞(Treg)の抑制に関する用量反応データを、数週間以内に取得可能
免疫細胞アッセイサービスのご紹介
アレイ化 B細胞スクリーニング
初代リンパ球における遺伝子発現調節の課題を、専門的なアウトソーシングによって克服してください。
当社のB細胞ゲノム編集プラットフォームにより、獲得免疫、炎症、自己免疫の研究を推進いたします。
初代リンパ球における遺伝子発現調節の課題を、専門的なアウトソーシングによって克服してください。
当社のB細胞ゲノム編集プラットフォームにより、獲得免疫、炎症、自己免疫の研究を推進いたします。
インフラを投資せず、標的同定から化合物評価まで対応する専門的なB細胞スクリーニングサービスにより、従来の創薬の限界を超えて先駆けましょう。高度なCRISPR技術と主要なB細胞サブタイプを横断する新規モダリティにより、未開拓領域への道筋を拓きます。
制御性B細胞の利点
制御性B細胞は、重要でありながら未開拓の治療領域です。これらの特殊な細胞はIL-10分泌を通じて免疫寛容を調整し、以下の重要な役割を果たします:
- 自己免疫疾患の進行
- がん免疫抑制
- 移植拒絶反応の動態
- 炎症反応の調節
当社のサイエンティストは、初代B細胞操作の技術的課題を克服し、細胞の生存率を維持しながら高い編集効率を達成する独自のプロトコルを開発しました。
エフェクターB細胞の精査
当社のゲノム編集技術は、B細胞の全段階にわたって適用可能です。確立された規制対応プラットフォームを基盤として、エフェクターB細胞に対しても最適化されたプロトコルを提供しています。エフェクターB細胞は、免疫活性化と抗体による防御の主要な担い手です。サイトカイン分泌と強力な抗体産生を通じて、以下の重要な役割を果たします:
- 病原体の中和
- 腫瘍監視機能の強化
- ワクチン応答の増強
- 自己免疫性炎症の促進
最適化されたワークフロー
当社の入念に最適化されたプラットフォームは、B細胞の本来の特性を保持する穏やかな分離技術により、細胞調製を改善します。
- 独自のエレクトロポレーションパラメータを活用し、細胞ストレスを最小限に抑えつつトランスフェクション効率を高めます。
- 高効率Cas9 RNPデリバリーによって精密な編集を実現し、オフターゲット効果を最小限に抑えることで、信頼性の高い遺伝子改変を提供します。
- フローサイトメトリーやHTRF™を含む複数のアッセイを通じて、編集された細胞を徹底的に特徴づける包括的な機能的検証を行います。
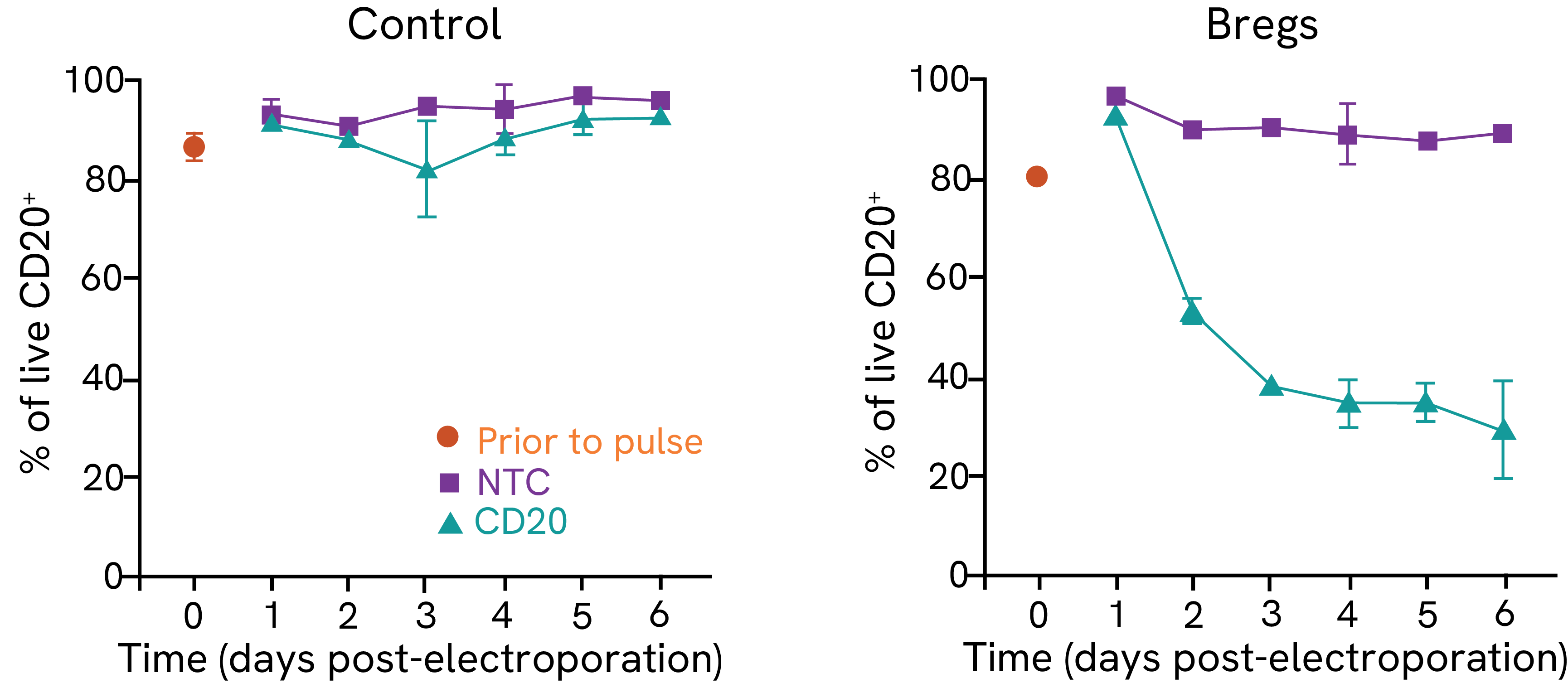
初代ヒトB細胞における効率的なゲノム編集。コントロールまたはBreg細胞に対し、MS4A1(CD20をコードする遺伝子)を標的とする化学合成crRNA-tracrRNA、またはNon-Targeting Control(NTC)とCas9を用いて編集を実施。化学合成crRNA-tracrRNAおよびCas9複合体の導入後、指定された時間におけるCD20陽性B細胞の割合を評価しました。
関連性のある初代Bリンパ球で真の生物学を捉える。
従来の細胞株では、ヒト初代B細胞が持つ生物学的な複雑性には対応できません。私たちのアレイ化スクリーニングプラットフォームは、複数ドナーにわたる自然なヒトの多様性を捉え、本来の免疫機能と応答を保持します。このアプローチにより、研究者は新たな標的の発見、遺伝的要因の検証、そして臨床応用に直結する知見をもとに、より予測性の高いモデルの構築が可能になります。
当社の高度な複合共培養技術についてもぜひご覧ください。当社の専門性が、皆様の研究をどのように変革できるかをご覧ください。
アレイ化骨髄系CRISPRノックアウトスクリーニング
初代免疫系骨髄細胞における遺伝子発現調節のパイオニア
単球およびマクロファージにおけるゲノム編集により、微小環境研究の次なるフロンティアへ到達しましょう。
初代免疫系骨髄細胞における遺伝子発現調節のパイオニア
単球およびマクロファージにおけるゲノム編集により、微小環境研究の次なるフロンティアへ到達しましょう。
創薬初期段階における遺伝子編集スクリーニングは、特に初代免疫細胞を扱う場合、高度な技術を有する研究者と多大なリソースを必要とします。Revvityの免疫細胞スクリーニング受託研究(CRO)サービスにより、創薬企業の皆様は単球およびマクロファージにおけるゲノム編集の専門性と非臨床サービスの能力を活用し、新たな治療可能性を切り拓くことができます。
なぜ単球およびマクロファージに対するゲノム編集なのか?
単球およびマクロファージは骨髄系細胞に属し、病原体認識、貪食、免疫応答の調節など、以下のような重要な役割を果たします。骨髄系細胞におけるゲノム編集は、疾患メカニズムの解明や新規治療標的の同定につながります。
しかしながら、これらの細胞タイプの生物学的特性により、化学合成sgRNAのトランスフェクション条件の最適化において、細胞のゲノム編集は依然として大きな課題となっております。
Revvityでは、当社の非臨床サービス担当科学者がDharmacon™ sgRNAのトランスフェクションプロトコルの最適化に成功しており、創薬企業の皆様がin vitroにおける生理学的微小環境研究の最前線に到達するための支援体制を整えています。
単球または単球由来マクロファージ(MDM)のゲノム編集
マクロファージは単球から分化し、免疫系において極めて重要な役割を担っています。主に以下の2種類に分類されます:
M1型単球由来マクロファージ(MDM):古典的活性化マクロファージとして知られ、炎症促進性応答において極めて重要です。炎症性サイトカインを産生し、微生物や腫瘍細胞を効果的に標的化することで、病原体に対する防御に寄与します。
M2型単球由来マクロファージ(MDM):代替活性化マクロファージとも呼ばれ、抗炎症反応と組織修復に不可欠です。抗炎症性サイトカインを産生し、創傷治癒や炎症の収束、線維化などを通じて組織再構築を促進します。
Revvityでは、骨髄系細胞のゲノム編集ワークフローを最適化し、編集効率を向上させています。主な利点は以下の通りです:
- 単球およびM0マクロファージにおける編集効率の向上
- 編集後の細胞培養条件を最適化(M-CSFまたはGM-CSF含有培地を使用
- 編集効率を最大化する最適なタイムポイントの特定
- M1/M2マクロファージへの効果的な分化誘導
- フローサイトメトリーによるM1/M2分化関連の細胞表面マーカー、およびHTRF™法によるサイトカイン放出を用いた包括的なエンドポイント解析
アレイ化T細胞CRISPRノックアウトスクリーニング
T細胞アレイスクリーニングによる治療ブレークスルーの未来を切り拓く
創薬の初期段階では、特に初代免疫細胞を用いたゲノム編集スクリーニングには多大なリソースを必要とします。Revvityの免疫細胞アッセイサービスのT細胞アレイ化ゲノム編集を活用し、治療法開発にお役立てください。
T細胞アレイスクリーニングによる治療ブレークスルーの未来を切り拓く
創薬の初期段階では、特に初代免疫細胞を用いたゲノム編集スクリーニングには多大なリソースを必要とします。Revvityの免疫細胞アッセイサービスのT細胞アレイ化ゲノム編集を活用し、治療法開発にお役立てください。
CRISPRノックアウト遺伝子スクリーニングは、創薬のダイナミックな分野で一般的に利用されるようになっています。治療標的を明らかにし、遺伝性疾患との関連性を理解する可能性を提供します。しかし、特にin vitroの制御された環境下では、遺伝子抑制が細胞機能に与える影響を十分に理解することが重要な克服すべき課題となっています。この課題は、免疫反応に不可欠な複雑な遺伝子相互作用を持つ初代免疫細胞などの非不死化細胞を操作する場合にはさらに困難になります。
T細胞におけるCRISPRノックアウトアレイ化スクリーニングとは?
CRISPR-Cas9ゲノム編集技術を用いてT細胞内の特定の遺伝子を系統的に破壊または「ノックアウト」する、特殊な遺伝子スクリーニングアプローチです。アレイ化スクリーニングでは、各ウェルでは単一の遺伝子がノックアウトされ、増殖(CTG)、表面および細胞内マーカー(FACS)、タンパク質放出の定量(HTRF™)などのマルチプレックスデータにより、その特定の遺伝子を詳細に解析することができます。ハイスループットプラットフォームによる自動化とタイムラインの短縮により、下流の機能アッセイで単一遺伝子ノックアウト細胞を使用することが可能になります。
CRISPRノックアウトのTリンパ球での応用
- CRISPRで発現調節した免疫系細胞における遺伝子の役割を調査
- CRISPRで発現調節した免疫系in vitroモデルにおける化合物の作用機序を評価
- 遺伝子と細胞の表現型の関係性を明らかにし、T細胞の挙動に及ぼす影響の研究
- 薬剤の表現型への影響を評価するための高度なミニチュア化されたプラットフォーム
RevvityのCRISPRノックアウトT細胞スクリーニングの特徴
Revvityでは、CRISPRノックアウト技術とT細胞ImmuSignature™アッセイの信頼性を組み合わせることで、従来のアプローチを超えるアプローチを可能にしています。この特徴的なサービスの組み合わせにより、当社のT細胞遺伝子スクリーニングの可能性が広がり、関連するin vitro免疫細胞機能評価とともに堅牢な統計解析を提供し、標的探索の研究を支援します。
- 薬剤の表現型への影響を評価するための高度なミニチュア化されたプラットフォーム
- 二重特異性(bi-specific)抗体、低分子化合物、モノクローナル抗体のスクリーニング用に設計
- HTRF™ テクノロジーによるサイトカイン放出の測定など機能的データ測定への拡張が可能
以下のリソースで詳細をご確認ください:

プール化T細胞CRISPRノックアウトスクリーニング
遺伝子機能喪失の解析によってリンパ球を制御する新規経路を発見
T細胞機能に重要な遺伝を同定することは、免疫疾患を標的とする上で極めて重要です。Revvityは、標的を評価するための正確なインサイトを提供し、皆様の研究成果のトランスレーショナルインパクトを高めます。
遺伝子機能喪失の解析によってリンパ球を制御する新規経路を発見
T細胞機能に重要な遺伝を同定することは、免疫疾患を標的とする上で極めて重要です。Revvityは、標的を評価するための正確なインサイトを提供し、皆様の研究成果のトランスレーショナルインパクトを高めます。
プール化スクリーニングは、費用対効果に優れたハイスループットな戦略であり、有望な治療標的を迅速に同定する上で大きな可能性を秘めています。Revvityのプール化T細胞CRISPRノックアウトスクリーニングは、ゲノム編集におけるコスト、範囲、スピード、再現性、精度といった課題に効果的に対応します。この技術革新は、T細胞バイオロジーの理解を深めるだけでなく、新たな治療標的の発見を促進します。
T細胞におけるプール化CRISPRノックアウトスクリーニングとは?
T細胞プール内の遺伝子機能を系統的に調べるための強力な方法です。このプロセスでは、幅広い遺伝子のコレクションを標的とするsgRNAライブラリーをデザインし、これらのsgRNAを含むレンチウイルスベクターを初代T細胞に形質導入します。sgRNAにガイドされたCas9酵素が標的遺伝子の二本鎖切断を誘導し、細胞修復の際に遺伝子がノックアウトされます。編集されたT細胞集団を増殖培養した後、遺伝子ノックアウトがT細胞の挙動に及ぼす影響を評価するための機能アッセイが実施されます。機能アッセイとして、増殖(CTG)、表面および細胞内マーカー(FACS)、タンパク質放出定量(HTRF™)、次世代シークエンシングが可能です。
CRISPRノックアウトのTリンパ球への応用
- 系統的な遺伝子探索により治療標的を同定
- CRISPRで発現調節した免疫系細胞における遺伝子機能の解析
- CRISPRで発現調節した免疫系in vitroモデルにおける化合物の作用機序を評価
- 遺伝子と細胞の表現型の関係性を明らかにし、T細胞の挙動に及ぼす影響の研究
Revvityのプール化CRISPRノックアウトT細胞スクリーニングの特長
プール化アプローチにより、多数の遺伝子の同時評価が可能となり、免疫関連疾患における機能的関連性を有する新規治療標的の発見が加速されることが期待されます。このスクリーニングは、CRISPR技術を活用し、初代T細胞における正確なゲノム編集を可能にすることで、再現性と信頼性を高めています。
- 薬剤の表現型への影響を評価するための高度なミニチュア化されたプラットフォーム
- 二重特異性(bi-specific)抗体、低分子化合物、モノクローナル抗体のスクリーニング用に設計
- 共培養や、HTRF™技術によるサイトカイン放出測定、NGS解析、バイオインフォマティクスなどの機能的データ測定を含む下流アッセイへの拡張が可能
以下のリソースから詳細をご覧いただけます:
混合リンパ球反応
ImmuSignature MLRアッセイで、臨床試験開始届(IND)申請の準備を整えましょう
免疫原性評価のためのMo-DCによる化合物スクリーニングおよびT細胞反応性スクリーニングについて、当社の専門性を持つスタッフが、プロジェクトの次のステップに向けた的確な意思決定を支援します。
ImmuSignature MLRアッセイで、臨床試験開始届(IND)申請の準備を整えましょう
免疫原性評価のためのMo-DCによる化合物スクリーニングおよびT細胞反応性スクリーニングについて、当社の専門性を持つスタッフが、プロジェクトの次のステップに向けた的確な意思決定を支援します。
混合リンパ球反応(MLR)アッセイとは?
混合リンパ球反応(MLR: Mixed Lymphocyte Reaction)アッセイは、抗原提示細胞とT細胞間の相互作用を調節して、リンパ球細胞の反応を活性化、抑制、または再分極させるような化合物を試験するためのプラットフォームです。このアッセイでは、治療薬やその他の免疫を調節する薬剤の有効性をテストできます。また、薬剤の安全性に関係する免疫学的反応性に関する重要な情報も得られます。
混合リンパ球反応アッセイは、あるドナーからのT細胞が、別のドナーからの抗原提示細胞(APC: antigen-presenting cells)の存在下で応答または増殖するという原理に依存しています。これは、非血縁間のヒト白血球抗原(HLA)のミスマッチで引き起こされます。HLAミスマッチは、T 細胞の免疫応答を刺激し、増殖を誘導します。 T細胞の表面にあるタンパク質が他の細胞の対となるタンパク質を認識して結合すると、免疫チェックポイントが活性化されます。これらのチェックポイントパスウェイは、T細胞が樹状細胞(DC)などのプロフェッショナルAPCに結合するときに関与します。
創薬プロジェクトで混合リンパ球反応アッセイを検討する必要があるのはなぜか?
MLRは、微小環境における薬剤に対する細胞の反応を測定するin vitro試験であり、化合物が体内でどのように相互作用するかを予測するのに役立ちます。医薬品開発において、このアッセイを用いてT細胞と抗原提示細胞間の相互作用を潜在的に増強、抑制、または再分極させる治療法の有効性をチェックできます。
RevvityのスタンダードMLRアッセイ
当社のone way MLRアッセイでは、同種異系(アロ)の単球由来樹状細胞(Mo-DC)を介して T 細胞の活性化を制御する薬剤をすみやかに同定できます。お客様のバイオ医薬品または低分子化合物を、in vitroの免疫微小環境で、半自動ハイスループット スクリーニングでテストします。
主な利点:
- 迅速で、ミニチュア化され、自動化に近い再現可能な384ウェル高スループットアッセイ
- 薬剤の安全性試験、がん免疫治療研究、および自己免疫疾患治療研究への応用が可能
- 堅牢な定量データ提出までのリードタイム:約4週間
- 複数の同種ドナー:ドナー間のばらつきに対処するため、複数のドナーからの初代T細胞および単球由来樹状細胞を使用
- 統計的に信頼性の高いデータセット(HTRF、AlphaLISA™、BioLegend LEGENDplex™)による複数の生理学的データ
以下のリソースから詳細をご覧いただけます:
マクロファージの極性化アッセイ
骨髄系細胞研究に新たな展開を
治療候補化合物がマクロファージサブタイプの分極に与える影響を研究しましょう。
骨髄系細胞研究に新たな展開を
治療候補化合物がマクロファージサブタイプの分極に与える影響を研究しましょう。
創薬研究支援に特化したサービスとして、当社は単球およびマクロファージ分化スクリーニングにおいて業界をリードしています。再現性の高い機能アッセイを行うために、当社の堅牢なM0、M1、M2サブセット生成プロトコルをご活用いただき、フローサイトメトリーやHTRF™、BioLegend LEGENDplex™、AlphaLISA™技術を使用したサイトカイン放出測定などのマルチプレックスデータをご取得ください。当社の骨髄系細胞の系統に関する専門性により、複数の分化段階で化合物スクリーニングを行うことができます。
分化および極性化したマクロファージの機能の探索
単球由来マクロファージ(MDM: Monocyte-derived macrophages)のタイプ0は、M1またはM2 MDMに効率的に極性化することができます。これらの特化型細胞タイプは、T細胞抑制を含む下流の機能アッセイに有用であり、免疫学における画期的な進歩の可能性を秘めています。
最先端のフローサイトメトリーと、上清中のタンパク質解析は、当社のサービスの中核を成しており、精度の高い実用的なデータを提供します。当社の細胞モデルと解析ツールを使用すれば、免疫反応の複雑なメカニズムを安心して研究することができます。経験豊富で専門知識を備えたスタッフとリソースを活用して、研究の新たな可能性を追求してください。
in vitroの単球由来マクロファージのサービス工程を用いて、がん免疫治療における細胞研究の拡大を
主な利点:
- 薬剤-表現型相互作用の評価のための先進的なミニチュア化プラットフォーム
- 二重特異性(bi-specific)抗体、低分子化合物、モノクローナル抗体のスクリーニングが可能
- HTRF™技術によるサイトカイン放出測定など、追加の機能的データ測定への拡張が可能
- CRISPRノックアウトアレイ化ゲノム編集プロジェクトとのシームレスな統合
T Cell Activationアッセイ
ImmuSignature TCAアッセイで、治療薬のT細胞に及ぼす影響を把握
ヘルパーT細胞と細胞傷害性T細胞の活性化と抑制に対する化合物の効果を明らかにし、創薬の非臨床フェーズへの移行を支援します。
ImmuSignature TCAアッセイで、治療薬のT細胞に及ぼす影響を把握
ヘルパーT細胞と細胞傷害性T細胞の活性化と抑制に対する化合物の効果を明らかにし、創薬の非臨床フェーズへの移行を支援します。
当社のT Cell Activationアッセイサービスにより、Tリンパ球から堅牢な定量データを取得し、組織の負担を軽減しながらリソースを有効活用できます。初代T細胞のアッセイには綿密な最適化、信頼性の高い細胞調達、確かなデータ解析を必要とします。経験豊富で専門知識を備えた当社のスタッフが、お客様のプロジェクトを検証済みのサービス工程で前進させ、お客様が必要とする免疫原性データを提供いたします。
T Cell Activationアッセイとは?
T Cell Activationアッセイは、T細胞の増殖能力に影響を与える化合物を評価するために設計されています。共刺激分子抗体の使用で、当社のT Cell Activationアッセイは、低分子化合物やバイオ医薬品などのお客様の目的化合物に対するCD4+およびCD8+T細胞サブセットの応答を模倣することができます。
創薬プロジェクトでT Cell Activationアッセイを検討する必要があるのはなぜか?
開発中の化合物のT細胞活性への効果を把握することは、がん免疫治療法への応用において必要不可欠です。T細胞活性化アッセイは、CD4+およびCD8+ T細胞サブタイプにおける細胞増殖や活性化を促進または阻害する効果を評価するための迅速なin vitro単培養系です。
T Cell Activationアッセイサービス
当社のT Cell Activationアッセイは、最適化された検証済みのミニチュア化されたスクリーニング条件のもと、T細胞の活性化または抑制に影響を与える化合物や新規免疫治療薬を迅速に同定します。お客様のバイオ医薬品あるいは低分子化合物を半自動化ハイスループットフォーマットで評価し、非臨床フェーズ入りを支援します。
主な利点:
- リードタイム:最短約3週間
- 迅速で半自動化された再現性のある384ウェルハイスループットアッセイ
- 腫瘍免疫学、自己免疫、および安全性評価への応用が可能
- 堅牢な定量データ
- 複数の同種ドナー:ドナー間のばらつきに対処するための、複数のドナー由来の高純度初代T細胞を使用
- 混合白血球反応(MLR)の補完的アッセイとして
以下のリソースから詳細をご覧いただけます:
iTreg 極性化(iTreg polarization)アッセイ
ImmuSignature iTreg 極性化アッセイで、誘導性制御性T細胞に対する治療薬の効果を検証
制御T細胞の研究は困難を伴います。免疫細胞を用いた化合物スクリーニングにおける当社の科学的専門性をご活用ください。確実な創薬を進めるためのデータを迅速に得ることができます。
ImmuSignature iTreg 極性化アッセイで、誘導性制御性T細胞に対する治療薬の効果を検証
制御T細胞の研究は困難を伴います。免疫細胞を用いた化合物スクリーニングにおける当社の科学的専門性をご活用ください。確実な創薬を進めるためのデータを迅速に得ることができます。
当社のiTreg極性化アッセイは、Naïve T細胞の制御性T細胞への極性化をコントロールできる治療薬候補を迅速に同定することができます。候補化合物は検証され最適化されたミニチュア化されたスクリーニング装置で実行され、一貫した信頼性の高いデータを提供されます。低分子化合物やバイオ医薬品は、半自動化されたハイスループットの機器構成で評価され、臨床入りのためのデータでお客様のプロジェクトをサポートします。
主な利点:
- 最短4週間でプロジェクトを完了
- 高速、半自動、再現性の高い384ウェルのハイスループットアッセイフォーマットで実施
- がん免疫治療研究、自己免疫疾患治療研究向けに設計
- ドナー間のばらつきに対処するため、複数のドナーからの初代T細胞を使用
- 堅牢な定量データ
iTreg極性化アッセイとは?
iTreg極性化アッセイは、誘導性制御性T細胞の表現型または機能における治療薬候補の効果の判断をサポートします。iTregは、免疫応答の制御と自己寛容の維持に不可欠な細胞です。
創薬プロジェクトでiTreg極性化アッセイを検討する必要があるのはなぜですか?
iTreg極性化アッセイは、iTregの極性化で発現する表現型を調節する治療薬候補の有効性を評価するための、迅速に実施できるin vitro単培養システムです。がん免疫治療研究への応用では、本アッセイで試験された化合物は、制御性表現型の誘導を制御することを実証することができます。抗炎症表現型へのTreg誘導を促進する治療薬は、炎症を抑制して病気を予防する能力を試験することができます。
iTreg極性化アッセイの主な応用例
創薬スクリーニングにおいて、iTreg誘導アッセイは、iTreg機能を損なう薬剤の可能性を評価することができます。これは、Tregの活性を抑制することで抗腫瘍免疫応答を高めることができるがんの治療に役立つ可能性があります。また、このアッセイは、自己免疫疾患や移植拒絶反応の治療に役立つ可能性のある、iTregの制御性表現型を強化する薬剤の有効性をテストすることができます。
以下のリソースから詳細をご覧いただけます:
iTreg抑制アッセイ
ImmuSignature TRPは、エフェクターT細胞の抑制に影響を与える候補を評価できます
誘導性制御性T細胞(iTreg)による T細胞抑制アッセイは、免疫微小環境に関する重要な洞察データを提供します。
ImmuSignature TRPは、エフェクターT細胞の抑制に影響を与える候補を評価できます
誘導性制御性T細胞(iTreg)による T細胞抑制アッセイは、免疫微小環境に関する重要な洞察データを提供します。
iTreg(誘導性制御性T細胞)の機能に対する化合物の影響を評価する、迅速かつ効率的なin vitro機能試験です。この試験は、エフェクターT細胞を抑制する能力を増強または抑制することにより行われます。このアッセイは、iTreg極性化アッセイと併用することで、化合物がiTregの生物学に及ぼす全体的な影響をより深く理解することができます。
主な利点:
- 最短6週間でプロジェクトを完了
- 高速、半自動、再現性の高い384ウェルのハイスループットアッセイフォーマットで実施
- がん免疫治療研究、自己免疫疾患治療研究向けに設計
- ドナー間のばらつきに対処するため、複数のドナーからの初代T細胞を使用
- 信頼性が高く定量的な高品質データの生成
iTreg抑制アッセイとは?
ImmuSignature iTreg 抑制アッセイは、エフェクターT細胞の抑制を調節できる可能性のある治療候補化合物を迅速に同定することができます。これらの候補化合物は最適化された小型のセットアップでスクリーニングされ、一貫性のある信頼性の高いデータが得られます。このアッセイは、低分子化合物やバイオ医薬品を評価の評価に特化しており、半自動のハイスループットフォーマットで実施され、臨床応用に向けたプロジェクトの前進を支援します。
創薬プロジェクトでiTreg抑制アッセイを検討する必要があるのはなぜか?
iTreg抑制アッセイは、iTregを介したエフェクターT細胞抑制の調節に対する治療候補化合物の影響を評価するために使用される、効率的なin vitro共培養法です。可溶性サイトカインによって駆動されるこの複雑な相互作用は、適応免疫系のエフェクター成分を調節することが示されています。がん免疫治療研究への応用では、本アッセイで試験された化合物は、iTregによるエフェクター細胞の制御を阻害する可能性を示すことができます。逆に、抗炎症性薬剤への応用では、持続的または強化された抑制効果が現れる可能性があります。
iTreg抑制アッセイの主な応用
薬剤スクリーニングの過程では、共培養システムにおける分極化した極iTreg細胞との相互作用を通じて、エフェクターT細胞の機能を妨げる薬剤の能力を評価するために、iTreg抑制アッセイが利用されます。この手法は、Treg活性の抑制が腫瘍に対する免疫応答を高める可能性があるがん治療に有望です。さらに、本アッセイでは、iTregの効力を高める薬剤の能力を評価することも可能であり、これは自己免疫疾患の治療に役立つ可能性があります。
以下のリソースから詳細をご覧いただけます:

カスタム免疫細胞プロジェクト対応力
私たちは、お客様の複雑な課題を解決します。
複雑な免疫細胞プロジェクトにおいて、リソースや専門知識が不足してお困りですか? 経験豊富で専門知識を備えた当社のスタッフと提携し、目標を明確化し、ロードマップを構築して、成果への道のりを加速させましょう。
私たちは、お客様の複雑な課題を解決します。
複雑な免疫細胞プロジェクトにおいて、リソースや専門知識が不足してお困りですか? 経験豊富で専門知識を備えた当社のスタッフと提携し、目標を明確化し、ロードマップを構築して、成果への道のりを加速させましょう。
当社と連携することで、プロジェクトの進捗、マイルストーン、重要な展開について定期的かつ頻繁にステータス更新を受け取ることができ、的確な意思決定やタイムリーなフィードバックが可能になります。
信頼性の高いデータに基づく、包括的かつ詳細な解析結果をご提供します。当社の厳格な解析手法により、正確で意味のある解釈が得られ、データに基づく意思決定と将来の戦略立案が可能になります。
免疫細胞カスタムスクリーニングの利点
- 効率性の向上:専門的な作業は当社が担当しますので、お客様は本来研究者の方が集中すべき研究に集中することができます。
- 専門知識へのアクセス:多様なスキルと知識を持つ当社のグローバルな人材プールを活用できます。
- スケーラビリティと柔軟性:ビジネスニーズに応じて業務を調整します。
- リスク共有:特定のリスクを当社の有能なスタッフに委ね、お客様の負担を軽減します。
- 時間の節約:時間のかかる作業を当社が担当することで、お客様は戦略的な活動に時間を充てることができます。
免疫細胞カスタムスクリーニングの利点
- 専任のプロジェクト管理チーム
- ミニチュア化された初代免疫細胞アッセイプラットフォーム
- ドナー仕様対応
- イメージングデータ
- ImmuSignatureアッセイの信頼性を活用
- 600種類以上の細胞株の広範なライブラリー
アッセイ開発分野の例
次の分野における初代免疫細胞のアッセイ開発については、当社にご相談ください:
- T細胞媒介性の腫瘍殺傷アッセイ
- B細胞の極性化および抑制アッセイ
- M1およびM2マクロファージの極性化
- NK細胞 抗体依存性細胞傷害活性(ADCC: antibody-dependent cell mediated cytotoxicity)アッセイ
- 抗体依存性細胞貪食能(ADCP: antibody-dependent cell-mediated phagocytosis)アッセイ
- 3D T細胞浸潤アッセイ
- アレイ化B細胞スクリーニング
- 補体依存性細胞傷害活性(CDC: Complement-Dependent Cytotoxicity)アッセイ
以下のリソースから詳細をご覧いただけます:
































